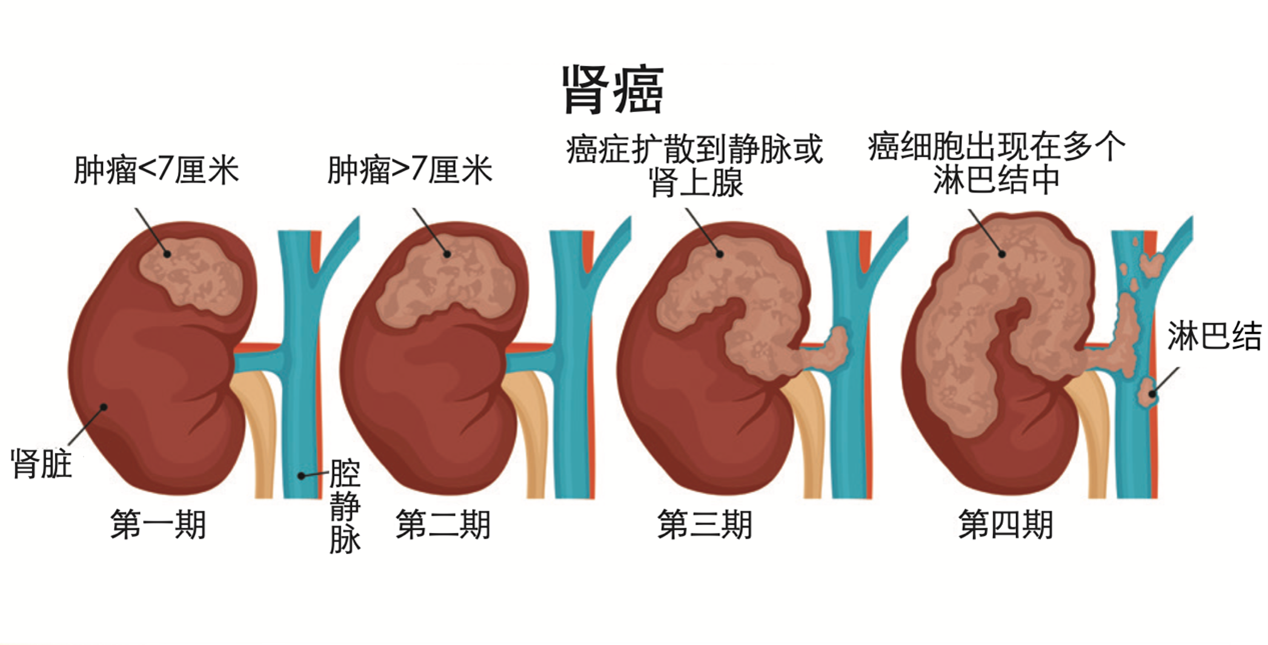
局部进展性肾细胞癌的治疗
局部进展性肾细胞癌既往称为局部晚期肾细胞癌,也是2017版AJCC肾细胞癌TNM分期系统的Ⅲ期病变,具体包括$T_1N_1M_0、T_2N_1M_0、T_3N_0M_0和T_3N_1M_0$。
根治性肾切除术
局部进展性肾细胞癌的首选治疗方法是根治性肾切除术(radical nephrectomy,RN)。
经典的RN切除范围包括患肾、肾周脂肪同侧肾上腺、肾周筋膜、从膈肌脚到腹主动脉分叉处淋巴结及髂血管分叉以上的输尿管。
当前观念已发生变化,不推荐术中常规行同侧肾上腺切除和区域淋巴结清扫。
不同术式之间的肿瘤学结果相当
(1)淋巴结清扫术:
一般而言,肾细胞癌患者发生血行转移更为常见,而发生区域淋巴结转移的病例绝大多数均已同时发生远处脏器转移,单独发生淋巴结转移者约占非转移性肾细胞癌病例的6.2%“。
目前仅有的一项前瞻性随机对照研究显示,常规淋巴结清扫的阳性率仅为4%。
影像学或术中怀疑淋巴结转移者,只有不到20%的病理证实确实为肿瘤转移。
- 在局部进展性肾细胞癌中,淋巴结清扫术的作用仍具争议。
- 目前多数研究观点认为,不推荐行常规淋巴结清扫,只有在术前影像学检查怀疑有淋巴结转移和(或)术中发现有肿大淋巴结时考虑进行淋巴结清扫术,但对于高危患者行淋巴结清扫可能有临床获益。
(2)同时性同侧肾上腺切除术
局部进展性肾细胞癌根治性切除术,有关切除肾上腺能否获得生存获益的研究较少,且多为回顾性研究,大部分研究样本量小,随访时间短,因此证据级别很低,无法得出确切结论。
一项美国梅奥医学中心的较大规模研究表明局部进展性肾细胞癌根治性肾切除术的同时常规切除同侧肾上腺并不能带来肿瘤学的获益,且不能防止术后对侧肾上腺转移,术后发生同侧和对侧肾上腺转移的风险相当中。
因此,对于局部进展期肾细胞癌,除非术前影像学检查发现肾上腺异常或术中发现同侧肾上腺异常考虑肾上腺转移或直接受侵,否则不建议行根治性肾切除术的同时常规切除同侧肾上腺。
肾细胞癌伴静脉癌栓的手术治疗
- 肾细胞癌中4%~ 10%伴有静脉癌栓”,未经治疗的肾细胞癌合并下腔静脉癌栓患者自然病程短,预后差,中位生存时间约5个月,1年肿瘤特异性生存率约29%
- 积极手术切除患肾和癌栓作为治疗肾细胞癌伴静脉癌栓患者的标准策略已被广泛接受”,且能使患者取得生存获益”。
- 最近的一项荟萃分析发现TNM分期、Fuhrman分级、肿瘤坏死和癌栓高度等与患者术后生存明显相关。
(1)肾细胞癌伴静脉癌栓的分级:
静脉癌栓分级对手术难度评估和手术策略的制订具有重要意义。目前应用最广泛的是2004年由美国梅奥医学中心(Mayo Clinic)提出的五级分类法,在开放手术时代发挥了重要作用,具体分级标准如下:
- 0级,癌栓局限在肾静脉内;
- Ⅰ级,癌栓侵入下腔静脉内,癌栓顶端距肾静脉开口处≤2cm;
- Ⅱ级,癌栓侵人肝静脉水平以下的下腔静脉内,癌栓顶端距肾静脉开口处>2cm;
- Ⅲ级,癌栓生长达肝内下腔静脉水平,膈肌以下;
- Ⅳ级,癌栓侵入膈肌以上的下腔静脉及右心房。
在微创手术时代,国内多家单位探索了微创手术下的静脉癌栓分级方法及手术策略“,以目前应用较多的“301分级”为例,其具体分类如下:
- 右肾静脉癌栓为0级;
- 左肾静脉癌栓根据是否超过肠系膜上动脉分为0a及0b级;
- 下腔静脉癌栓分为四级:
- 第一肝门以下的下腔静脉癌栓为工级;
- 第一肝门以上至第肝门Ⅱ级;
- 第二肝门至膈肌水平为Ⅲ级,
- 膈肌以上为IV级
开放根治性肾切除联合静脉癌栓取出术是最常用的术式。部分单位已经开展腹腔镜下或机器人辅助根治性肾切除术联合静脉癌栓取出术。为了减少术中癌栓脱落风险,总体原则是先处理静脉癌栓再切除患侧肾脏及肿瘤。
- 对于腹腔镜和机器人手术而言,右侧肾细胞癌伴下腔静脉癌栓可采取左侧卧位同时切除癌栓及右肾
- 而对于左侧肾细胞癌伴下腔静脉癌栓,可先采取左侧卧位处理下腔静脉癌栓,再更换右侧卧位处理左肾。
- 对于肝后段癌栓,第一第二肝门血管是重要的解剖学标志,不同解剖学特征的下腔静脉癌栓应采取不同的血管阻断顺序和重建策略。
- 对于Ⅳ级癌栓,建议常规建立体外循环,如癌栓进人右心房,则需阻断上腔静脉及下腔静脉回流后切开右心房取栓。
针对部分未侵人右心房的Ⅳ级癌栓,基于心包内控制技术的免体外循环是可行的对于复杂病例,特别是Ⅲ~Ⅳ级癌栓患者,推荐多专科协作,可降低围手术期并发症发生率和死亡率。
下腔静脉癌栓切除术包括切开取栓及离断两种手术策略,其中下腔静脉切开取栓术是最常用的术式。
下腔静脉离断术的适应证为下腔静脉完全梗阻且侧支循环充分代偿,其他影响因素包括癌栓高度、肿瘤侧别、静脉壁侵犯程度及范围、近、远心端血栓形成等。
下腔静脉癌栓切除术中针对难以一期修复的长段静脉缺损,对于有经验的单位可选择人工血管替代。一项关于静脉梗阻与代偿的三维影像重建研究提示:在下腔静脉渐进性梗阻过程中,除了通过天然属支(腰静脉、生殖静脉,奇静脉/半奇静脉)回流外:双侧肾静脉还可通过肾周静脉/肾包膜静脉与肠系膜上/下静脉、门静脉、膈下静脉建立新的侧支循环”。
(2)肾细胞癌伴静脉癌栓围手术期处理
1)肾细胞癌伴静脉癌栓术前是否需要行肾动脉栓塞尚有争议。
有研究表明肾动脉栓塞具有阻断肿瘤血供、减少术中出血、缩小肿瘤体积、降低癌栓高度等潜在优势。也有研究指出,术前肾动脉栓塞不能改善围手术期结果或提高患者生存获益,甚至增加肾死综合征及目标外脏器意外栓塞的风险。
一般认为,对于右侧肾细胞癌伴下腔静脉癌栓患者,不推荐常规行术前肾动脉栓塞术,但对于巨大肿瘤、淋巴结包绕肾血管等复杂情况可选择术前动脉栓塞。在腹腔镜或机器人手术中,对于左侧肾细胞癌伴下腔静脉癌栓患者,推荐术前左肾动脉栓塞或术中先行左肾动脉离断。
2)下腔静脉癌栓合并血栓并不罕见,文献报道其发生率为23.4%。
癌栓近心端血栓脱落是围手术期肺栓塞的主要原因,远心端血栓可达髂血管分叉甚至下肢静脉,增加了术中完整取栓的难度。
对于合并血栓的静脉癌栓患者,推荐术前行抗凝治疗。
目前尚无静脉癌栓围手术期标准抗凝治疗方案,美国临床肿瘤协会(ASCO)和NCCN治疗指南均建议将低分子肝素作为肿瘤相关血栓长期治疗的首选药物。
有研究报道,从诊断发现癌栓和血栓时开始用药,推荐使用低分子量肝素抗凝治疗,用药至手术前24小时,维持国际INR值为2~3,术后48小时如无活动性出血可恢复抗凝治疗,最长可维持使用6个月
3)术前是否需要放置下腔静脉滤网存在争议。
滤网放置可预防严重肺栓塞,但滤网放置过程中可能会导致癌栓脱落,并增加手术取栓的难度”,不推荐常规放置。
局部进展期肾细胞癌相关药物治疗
(1)局部进展期肾细胞癌术前新辅助治疗:
由于缺乏大样本前瞻性随机对照临床研究证据,局部进展期肾细胞癌的新辅助治疗尚无标准方案。
多项Ⅱ期临床研究证实术前新辅助靶向或靶向联合免疫治疗可降低局部进展性肿瘤分期,降低手术难度,改善患者预后。术前新辅助靶向治疗下腔静脉癌栓的研究显示,44%~76%的患者癌栓高度降低,12%~ 43%的患者癌栓降级。其中一项研究结果显示,术前应用阿昔替尼可显著缩小癌栓体积并减少术中出血量,癌栓降级率达42%。对于高分级下腔静脉癌栓、巨大肾肿瘤伴或不伴邻近脏器侵犯等复杂病例,术前新辅助治疗有可能降低手术难度,提高手术成功率。
(2)局部进展期肾细胞癌术后辅助治疗:
局部进展性肾细胞癌行根治性肾切除术后尚无标准辅助治疗方案。
目前尚无随机亚期试验的数据表明辅助治疗可提供生存获益。由于肾细胞癌对放、化疗不敏感,不推荐术后对瘤床区域进行常规放、化疗。
研究数据显示术后辅助白介素-2/干扰素、化疗或者激素治疗高复发风险肾细胞癌均未能延长患者总生存”。在靶向治疗时代,已经有四项随机对照研究报道了高复发风险肾细胞癌术后靶向治疗的结果,ASRURE和SORCE研究均为阴性结果,S-TRAC研究证实舒尼替尼辅助治疗可改善无病生存,但总体生存的数据未达统计学差异。PROTECT研究显示术后辅助培唑帕尼800mg可改善患者的无病生存率,但600mg剂量无统计学意义。
因此分子靶向治疗作为局部进展期肾细胞癌的辅助治疗未能获得生存获益(证据水平1b)。随着以免疫检查点受体为靶标的肿瘤免疫治疗的兴起,多项针对局部进展期肾细胞癌术后免疫维持治疗的临床试验尚在进一步研究中。