转移性前列腺癌的治疗与随访
(一)概述及疾病评估
1.概述
转移性前列腺癌(mPCa)是严重影响前列腺癌患者预后的重要疾病阶段。在欧美人群中mPCa仅占新发前列腺癌的5%~6%”,而在我国这一比例则高达54%口。欧美mPCa患者的5年总体生存率约为30%,而我国有限的数据显示,国人mPCa患者5年总体生存率为40%~52%,显示出比欧美人种更好的预后。
雄激素剥夺治疗(androgen deprivation therapy,ADT)是mPCa最广泛使用的基础治疗方法,近年来此领域中一系列突破性的进展(主要是新型内分泌治疗药物或化疗药物的联合使用)更新了传统ADT的治疗观念,并改善了mPCa的总体治疗效果。
2.诊断及疾病评估
转移性前列腺癌的患者通常因PSA升高、骨痛或病理性骨折被发现,原发灶或转移病灶经病理确诊后,需要通过CT、MRI、骨扫描、PET等影像检查,以及肿瘤相关血生化指标检测等手段全面评估肿瘤负荷状态。确诊时部分基线指标以及ADT治疗后PSA变化等可作为预测治疗效果的判断因素,国内外一些评估模型也有助于预测整体预后辅助治疗决策的选择。
(1)肿瘤负荷及风险评估:
mPCa患者的转移病灶数目及肿瘤负荷等与治疗预后有关,随着近年来几项大型临床研究结果的公布,针对mPCa患者的评估分层方法逐渐广泛应用于临床。
“寡转移”(Oligo-metastatic)前列腺癌的概念最早在1995年由Hellman和 Weichselbaum提出,指从局限性前列腺癌进展为广泛mPCa之间的一个特定疾病阶段,其预后也界于二者之间”。
目前,关于“寡转移”的定义尚无统一标准,不同文献报道中,对转移病灶数目的定义存在差异,部分文献还将转移病灶的部位、转移时间(同时或异时转移)及患者去势状态等作为定义标准的组成部分”。
高转移负荷(high-volume disease,HVD)与低转移负荷(1ow-volume clisease,LVD)的概念源于近期几项大型临床研究:
- HVD定义为内脏转移,或骨转移病灶>4处,其中至少1处在脊柱或骨盆以外
- LVD定义为无内脏转移且骨转移病灶≤3处。
高危疾病(highriskdisease,HRD)与低危疾病(low risk disease,LRD)的分类方法也源于大型临床研究,前者指满足以下3个危险因素中的2个:Gleason评分>8分,骨转移病灶>3处,存在内脏转移,后者为具备不超过1个上述危险因素。 CHAARTED、STAMPEDE、LATITUDE等几项临床研究显示,对于转移性激素敏感性前列腺癌mHSPC)患者,单纯去势治疗联合多西他赛或阿比特龙,可显著降低HVD或HRD患者的死亡风险,延长影像学无进展生存时间,推迟PSA进展时间“STAMPEDE研究的最新分析结果还显示,LVD患者仍然能从联合阿比特龙治疗中获得生存获益”。而另一项 ENZAMET研究显示单纯去势联合恩扎卢胺可显著降低LVD患者的疾病进展及死亡风险u91
(2)预期寿命及体能评估:
与局限性和局部进展期前列腺癌患者相似,mPCa患者预期寿命和体能状态是影响临床治疗策略制定的重要因素。通常采用G8标准对患者包括合并症、营养状态、认知及体能状态(ECOG评分)等因素进行综合评估。
(二)总体治疗原则及选择策略
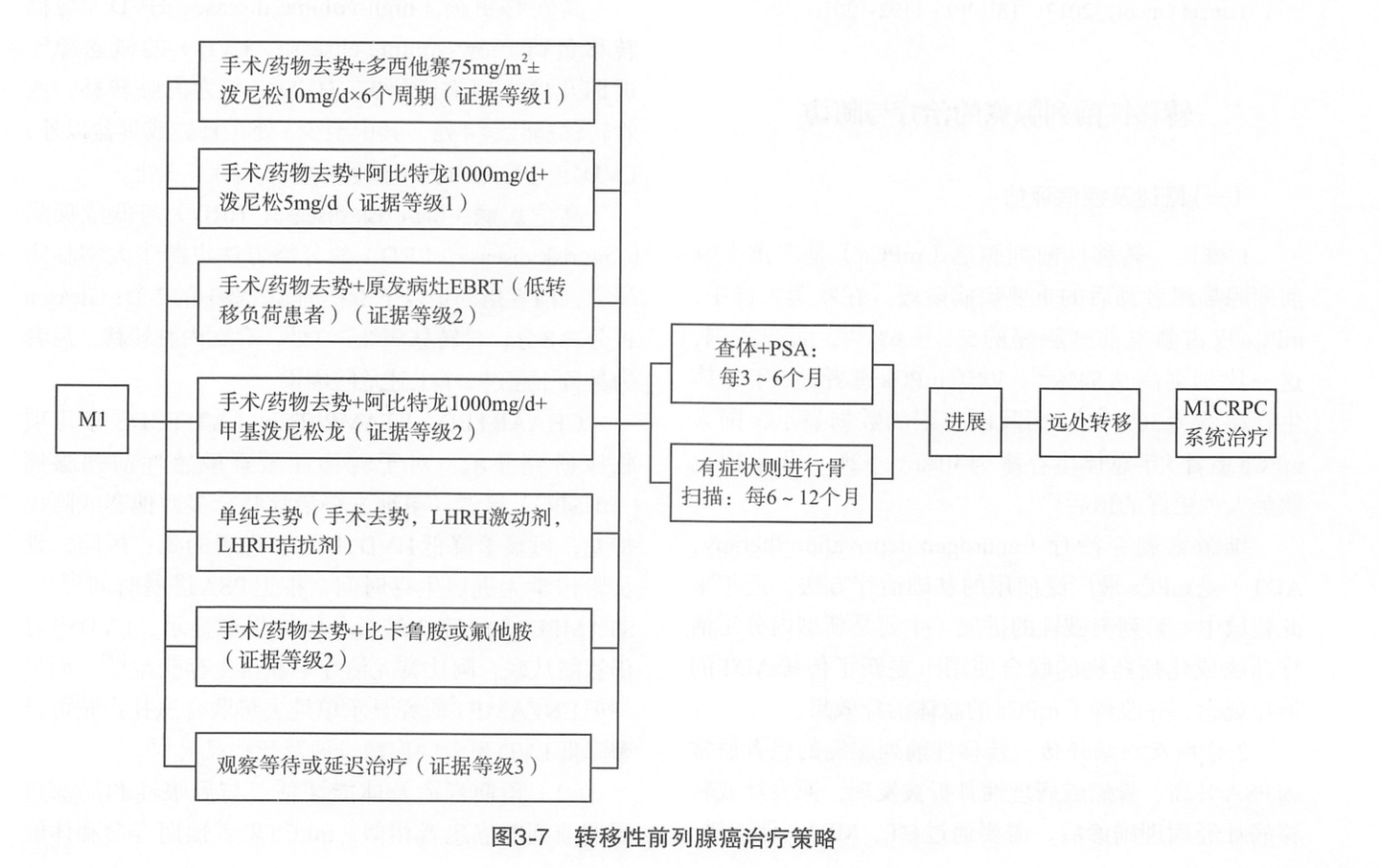
除了极少数无症状性mPCa可以选择“观察等待”(或延迟治疗)的方式以外,几乎所有mPCa患者需要接受治疗(图3-7)。
ADT是mPCa最主要的标准治疗方式,也是各种新型联合治疗方案的基础,且常需贯穿患者后续治疗的始终。
ADT治疗包括多种实施方案,其中单纯去势(外科或者药物去势)是最广为接受的核心治疗方式。随着近年来多种新型内分泌治疗药物的出现,在单纯去势治疗基础上,联合使用这些新型药物取得了显著的临床获益,并成为ADT治疗的未来趋势。 尽管如此,各种新型的联合用药方案带来的相关药物毒性反应及经济负担需要加以重视,并作为临床决策重要的参考。未来,针对转移性前列腺癌的分层治疗将成为保证疗效、平衡毒性不良反应和节约医疗资源的总体原则,并成为今后临床探索的重点。 针对mPCa原发病灶或转移病灶的局部治疗临床获益尚未获得充分证据,多个前瞻性研究似乎提示该种治疗对进一步改善预后具有积极作用。
针对mPCa的治疗方案多样(图3-7),包括:单纯去势,包括:
- ①手术去势及药物去势(促黄体激素释放激素激动剂(LHRHa);或促黄体激素释放激素拮抗剂luteinizing hormone-releasing hormone antagonist );
- ②去势联合多西他赛;
- ③去势联合新型内分泌药物治疗(阿比特龙或恩扎卢胺);
- ④去势联合传统非甾体类抗雄激素药物(氟他胺或比卡鲁胺);
- ⑤观察等待watchful waiting,WW)或延迟治疗
1.观察等待或延迟治疗
(1)定义:mPCa的WW或延迟治疗是指在少数患者中密切监测mPCa的疾病进程,在出现肿瘤进展或临床症状明显时再给予治疗。 (2)适应证及禁忌证:对于无症状或强烈意愿拒绝接受药物治疗的患者可考虑进行观察等待或延迟治疗。由于转移性患者的平均中位生存时间仅40个月左右,因此对于大多数患者可以采取WW或延迟治疗时间往往十分有限。需要注意的是,由于未接受系统性内分泌治疗,在等待治疗期间患者存在疾病进展甚至死亡风险。因此,拟采用延迟治疗患者须进行密切随访,临床医师需谨慎选择适宜的患者
2.ADT
1941年,Huggins和Hodges发现手术切除双侧睾丸可延缓mPCa的进展,首次证实了前列腺癌对雄激素去除的反应性,奠定了前列腺癌ADT的基础。任何去除雄激素或抑制雄激素活性的治疗方法统称为ADT,也称前列腺癌的内分泌治疗。ADT治疗从作用机制上分为以下4类
- 1)手术去势:通过双侧睾丸切除术(毁损雄激素分泌器官)达到阻断雄激素分泌的作用
- 2)药物去势:通过药物抑制LHRH分泌,继而抑制睾丸分泌雄激素,常用药物包括LHRHa和促黄体激素释放激素拮抗剂(luteinizing hormone-releasinghormone antagonist)两类。
- 3)抗雄激素类药物(雄激素受体拮抗剂):分为甾体类雄激素受体拮抗剂如醋酸环丙孕酮等,以及非甾体类雄激素受体拮抗剂,如氟他胺、比卡鲁胺恩扎卢胺、阿帕他胺等。
- 4)抑制雄激素合成的药物:包括酮康唑、阿比特龙等。 由于在阿比特龙、恩扎卢胺、阿帕他胺等新型内分泌治疗的药物出现之前,国际上主流的ADT治疗方式多为单纯药物去势或手术去势,故近年来多数国际文献中常以ADT来指代外科或药物去势。
(1)单纯去势治疗
1)手术去势治疗:双侧睾丸切除术是一种简单成本低、不良反应小的手术方式,可以通过局部或全身麻醉完成。手术后,血清睾酮水平快速下降,通常在12小时以内,患者睾酮可达到去势水平。当患者病情需要尽快降低睾酮(例如,即将发生脊髓压迫)或者当药物去势在经济、患者依从性方面存在困难时,双侧睾丸切除术是一种合适的选择。但与药物去势相比,手术去势可能会给患者带来负面的身心影响。通过改进睾丸切除术可以一定程度地减轻患者的心理影响,具体方式包括置入睾丸假体和包膜下睾丸切除术(保留白膜和附睾的完整性)等,从而维持近乎正常的阴囊外观。
2)药物去势治疗:药物去势的原理是通过影响下丘脑-垂体-性腺轴,减少睾丸产生的雄激素。常用药物包括促黄体激素释放激素激动剂和促黄体激素释放激素拮抗剂。
①促黄体激素释放激素激动剂(LHRH agonist,LHRHa):促黄体激素释放激素(LHRH),亦称促性腺激素释放激素(GnRH),在下丘脑中合成,能够促使垂体分泌卵泡刺激素(FSH)和黄体生成素(LH)。人工合成的LHRH具有很强的受体亲和力,且难以被酶降解,其作用效力约为天然LHRH分子的100倍。在采用LHRH激动剂治疗一周后:LHRH的受体会出现下调,垂体产生的LH和FSH也随之下降;在应用3~4周后,血清睾酮降至去势水平。
目前临床上应用的LHRHa包括亮丙瑞林、戈舍瑞林、曲普瑞林、布舍瑞林和组氨瑞林等。这些药物包含多种剂型(1,3,6个月剂型和1年期剂型等)是目前药物去势治疗的主要药物。目前尚没有1级证据支持哪种LHRHa效果更好。
在开始应用LHRHa治疗时,LHRHa与受体结合能够引起LH和FSH的释放,进而引起睾酮水平的突然上升导致闪烁现象(fare-up),这种现象可能会刺激前列腺癌的生长,并引起骨痛、膀胱出口梗阻或其他前列腺癌相关症状加重。为了减少这种睾酮水平突然上升的现象发生,在应用LHRHa的初期,至少应联用经典非甾体抗雄激素药物1~4周。
与睾丸切除术相比,LHRHa不会引起手术去势相关的心理问题,在停药后性腺功能减退相关的症状会有所改善具备间歇药物去势治疗的条件。 LHRHa与手术去势相比,在前列腺癌患者预后方面并没有差异。一项纳人10项临床试验(包含1908例前列腺癌患者)的Meta分析比较了LHRHa与睾丸切除术,两者在患者总生存率、疾病进展以及治疗失败时间方面无明显差异。
②促黄体激素释放激素拮抗剂(LHRHantagonist):LHRH拮抗剂如地加瑞克,能够通过与LHRH受体迅速结合,降低LH和FSH的释放,继而抑制睾酮水平。由于LHRH拮抗剂不会在治疗初始阶段刺激睾酮分泌,因此能够避免睾酮水平突然升高导致的疾病加重现象。但是,LHRH拮抗剂发生皮肤注射反应的比例较高,临床应用前需向患者特别交代说明, 由于缺少长效剂型,地加瑞克需每月进行注射,地加瑞克的标准用量为首月240mg,之后每月80mg维持。研究显示,多数患者应用地加瑞克可以在3天内将睾酮降至去势水平,并且在后续的12个月维持用药期间,睾酮水平能够被抑制并得以维持。由于地加瑞克缺少长期应用的疗效数据,目前尚不能明确LHRH激动剂和地加瑞克之间的效果差异。LHRH拮抗剂治疗效果是否优于LHRH激动剂有待进一步研究证实。
总体而言,单纯去势治疗在mPCa治疗中的重要价值早已得到证实和认可。早在2000年的一项汇集27项临床研究的荟萃分析中显示,接受单纯去势治疗的患者5年生存率可达到24.7%,其疗效与联合接受甾体类抗雄药物治疗的患者没有差别;与联合接受非甾体类抗雄药物患者疗效间差异有统计学意义但差距很小。尽管受到新型联合治疗方案的冲击,由于其简单、经济、有效,单纯去势治疗仍然是mPCa的标准治疗方案选择之一。目前尚没有高等级循证医学依据证明哪种单纯去势治疗方案效果更好。
(2)单纯抗雄激素药物治疗
1)甾体类抗雄激素类药物:
甾体类抗雄激素类药物主要是羟基孕酮的人工合成衍生物。主要包括醋酸环丙孕酮、醋酸甲地孕酮、醋酸甲羟孕酮等,其中醋酸环丙孕酮应用相对较多。醋酸环丙孕酮通过阻断雄激素受体和抑制雄激素合成而产生作用。一项RCT研究比较了醋酸环丙孕酮和LHRH激动剂,结果显示醋酸环丙孕酮组的OS较差。另外一项RCT研究比较了醋酸环丙孕酮和氟他胺单药方案治疗mPCa的效果,结果显示两者在CSS和OS方面均未见明显差异 此类药物除了会导致继发于去势之后的不良反应外,还存在心血管毒性(例如醋酸环丙孕酮)和肝毒性。
2)非甾体类抗雄激素类药物:
非甾体类抗雄激素类药物可与AR结合,但不会抑制雄激素的分泌。此类药物具有肝毒性,应用期间应监测患者的肝功能变化。目前临床上此类药物主要包括氟他胺、比卡鲁胺、尼鲁米特、恩扎卢胺和阿帕他胺。 ①氟他胺:氟他胺是一种前体药物,药物半衰期为5~6小时,几乎完全经尿液排出。目前推荐的应用剂量为750mg/d。氟他胺引起的不良反应有腹泻、恶心和呕吐,虽然肝毒性不常见,但可能会产生严重肝毒性,甚至出现肝衰竭而导致患者死亡,治疗期间需监测肝功能B37.81 ②比卡鲁胺:比卡鲁胺的单药方案为150mg/d,与ADT联合治疗时的给药方案为50mg/d。该药物的主要不良反应包括男性乳腺发育症(70%)和乳房疼痛(68%)。但相比于尼鲁米特和氟他胺,比卡鲁胺在药物安全性和耐受性方面仍然存在明显优势,并且其与雄激素受体的亲和能力是尼鲁米特和氟他胺的4倍,更好地保证了其对AR的竞争抑制能力。另外有研究表明,相比于LHRH激动剂和LHRH拮抗剂比卡鲁胺单药方案能够提供更好的骨骼保护作用。
③尼鲁米特:目前尚缺乏尼鲁米特单药方案的临床证据,单药方案尚未得到批准。除了抗雄激素特性引起的不良反应外,尼鲁米特的其他不良反应有暗适应延迟、恶心、可逆的肝转氨酶升高、酒精不耐受等,甚至出现致命性的间质性肺炎。鉴于以上原因,尼鲁米特在临床上应用较少, ④恩扎卢胺:一种新型选择性雄激素拮抗剂,可通过识别AR的配体结合域,抑制雄激素-AR的结合;抑制活化AR的核转运以及抑制AR与DNA的结合,从而阻断AR介导的转录中。未见单药使用研究,多与手术/药物去势治疗联用(见后文)。 ⑤阿帕他胺:另一种在结构和药代动力学与恩杂鲁胺极其相似的新型雄激素拮抗剂,但其对AR的亲和力更高,且不易透过血脑屏障。未见单药使用研究,多与手术/药物去势治疗联用(见后文)。 有关单独使用传统非甾体类抗雄药物进行雄激素剥夺治疗的荟萃分析则显示:与单纯去势(手术去势或药物去势)治疗mPCa的疗效相比,传统非甾体类抗雄药物的单药治疗在总生存期、疾病进展、治疗抵抗以及毒性反应等方面均存在劣势。因此对于转移性前列腺癌,不推荐采用非甾体类抗雄激素单药方案进行治疗。
(3)以药物或手术去势为基础的联合治疗方案
1)联合多西他赛化疗:
多项有关药物/手术去势联合多西他赛化疗的RCT研究比较了单纯去势和药物/手术去势联合多西他赛(75mg/m,每3周1次加泼尼松10mg/d)治疗mPCa的临床疗效“14.I549ICHAARTED试验和STAMPEDE试验结果均显示相比于单纯去势,药物/手术去势联合多西他赛化疗显著改善高肿瘤负荷mPCa患者的总体预后。因此,药物/手术去势联合多西他赛化疗应作为mPCa:特别是高肿瘤负荷患者的标准治疗方案选择。
2)联合新型内分泌药物治疗
①联合使用阿比特龙:阿比特龙为CYP17抑制剂,它的作用机制是阻断睾丸、肾上腺和前列腺癌肿瘤细胞产生的雄激素。LATITUDE试验和STAMPEDE试验结果显示,相比于单纯去势治疗,药物/手术去势联合阿比特龙(1000mg/d)加泼尼松(5 mg/d)治疗组能显著改善患者的预后。尽管改善生存的差异不大,但STAMPEDE研究的最新分析结果仍然显示去势联合阿比特龙可以延长低危mPCa患者的总体生存。因此,药物/手术去势联合阿比特龙加泼尼松应作为mPCa患者的标准治疗方式。 ②联合使用恩扎卢胺或阿帕他胺:最新研究表明新型非甾体类抗雄药物恩扎卢胺(160mg/d)或阿帕他胺(240mg/d)联合去势亦能显著改善mHSPO患者预后。在ENZAMET研究中,低肿瘤负荷患者相较高肿瘤负荷和既往接受过多西他赛为基础化疗的患者,能从联合治疗中获得更多生存获益,但该研究的随访时间较短,低肿瘤负荷患者是否从联合治疗中最终获益尚需更长时间更大样本量的临床数据。这些新型抗雄药物联合治疗的临床研究数据与阿比特龙相似,已获得FDA批准,成为mPCa患者治疗的标准治疗方案之一。 ③联合使用氟他胺或比卡鲁胺:去势治疗与氟他胺或比卡鲁胺联合使用包括两种情况。
- 一种是在使用LHRH激动剂类药物开始阶段短时间(1~4周)联用,有助于减少由于睾酮水平一过性升高导致疾病症状加重的情况发生
- 另一种是将药物去势与氟他胺或比卡鲁胺长程联合使用。
值得注意的是,这种联合用药的方案在国内仍有较广泛的使用。来自欧美人群的荟萃分析结果显示,采用去势联合这类非甾类抗雄激素药物的治疗方案,能够较单纯去势治疗延长患者3%的5年生存率,尽管差异具有微弱的统计学意义,但国外各大指南仍然在权衡疗效和安全性的平衡后,已不再推若这种联合用药方案。
然而,此种传统联合治疗方案在国内(乃至一些亚洲国家)仍有使用,近期一些回顾性研究及荟萃分析显示,这种方案或能为部分mPCa患者带来一定生存获益(多数研究为国内样本人群或加入了相当比例的国内人群研究结果 ),但具体获益人群筛选,以及真实获益情况尚待进一步研究证实。
基于现有证据并结合国内诊疗现状,药物/手术去势联合氟他胺或比卡鲁胺仍可作为治疗mPCa的可选方案之一
(4)间歇性与持续性药物去势的选择:
接受长期药物去势治疗后,由于睾酮水平持续维持去势水平,患者面临代谢综合征、贫血、骨质疏松、情绪异常等诸多不良反应。如果停止药物去势,患者的睾酮水平多会逐渐恢复至正常水平,不良反应随之改善。因此,相对于长期持续性单纯去势治疗概念外,提出了间歇性药物去势的概念,即指在对患者进行一段时间药物去势后,对治疗有效的患者撤除去势药物治疗,然后当出现疾病复发或进展的证据时再恢复药物去势治疗,目的是降低由药物去势带来的不良反应。
一项大规模前瞻性非劣性研究(SWOG9346)的结果提示,间歇性药物去势在治疗mPCa患者的生存数据较持续性药物去势存在劣势。多项荟萃分析结果则显示间歇性药物去势和持续性单纯去势治疗对于mPCa的疗效无明显差异。2017年,一项基于人群的回顾性研究显示,间歇性药物去势可以明显降低去势治疗所带来的心血管事件、心力衰竭及病理性骨折等不良反应。
因此,尽管间歇性药物去势无法在疗效上超越持续性单纯去势治疗,但对提高患者的生活质量,减轻去势治疗相关副作用具有重要临床应用价值,值得临床医师在治疗决策上认真考虑。鉴于以上结果,间歇性药物去势治疗应持谨慎态度,对于无症状患者,在充分告知获益和风险后,可对有积极意愿且依从性较高的患者采用。
但临床采用间歇性药物去势治疗时,需特别注意以下事项:
- ①间歇性药物去势是间歇性内分泌的治疗基础,因而间歇性内分泌中所使用的药物应具有明确的去势作用;
- ②诱导期不要超过9个月;
- ③当患者有明确PSA反应后才能中断治疗;
- ④如果患者出现临床进展或PSA升高超过经验性阀值时,应重新开始治疗。再次治疗应用相同方案至少3~6个月
- ⑤必须严密随访,每3~6个月检测PSA;
- ⑥后续的周期治疗采用相同的原则,治疗持续到出现去势抵抗的证据时结束。
(三)针对原发灶、转移灶的局部治疗
1.原发灶治疗
近10余年来,多项回顾性研究报道了转移性激素敏感性前列腺癌行原发灶手术或者放疗,给患者带来临床获益。然而,并非所有患者的原发灶治疗都能改善预后。
推荐对于年轻、一般状况良好、低转移负荷的mPCa患者进行原发灶放疗。减瘤性前列腺癌根治术能否取得与放疗类似的结果,还有待前瞻性临床研究结果证实,建议采取临床研究的方法谨慎开展。 此外,转移性激素敏感性前列腺癌原发灶治疗能降低发展至去势抵抗阶段出现排尿困难及血尿等下尿路症状的风险。尽管文献报道前列腺手术或者放疗的并发症与局限期前列腺癌的相当,但原发灶治疗可能引起的泌尿道或者肠道并发症仍需重视,需要同患者充分沟通、权衡利弊、谨慎实施。
2.转移灶治疗
对于转移灶将导致脊髓压迫和病理性骨折等紧急并发症的患者,建议行转移灶部位手术和/或放射治疗。 前列腺癌根治性治疗后寡转移的患者(<3个转移灶),转移灶局部治疗可以延迟全身治疗的时间,然而,还不清楚转移灶局部治疗能否改善生存期。
(四)治疗期间随访原则及监测项目
随访目的是确保治疗依从性、评估疗效及监测不良反应。随访内容包括临床随访、血液学检查(包括PSA、睾酮、血红蛋白及肝肾功能等)、影像学检查和监测代谢相关并发症等,推荐在内分泌治疗开始后第3个月和第6个月进行初步随访评估。